A Anvisa determinou a apreensão e inutilização das unidades do lote 1310710-4 do medicamento Biomag 15mg (cloridrato de sibutramina). A resolução RE 910/17 a qual indica essa medida sanitária foi publicada no Diário Oficial da União (DOU) nesta terça-feira (04/04). O fabricante do medicamento Biomag 15mg, Aché Laboratórios Farmacêuticos S.A., que detém o registro do produto, informou que não fabricou o lote 1310710-4 (validade 10/2018). Por se tratar de um caso de falsificação, a Agência Sanitária determinou, em todo o território nacional, a apreensão e inutilização de todas as unidades do lote em questão. Desodorante não registrado O comércio do…
Produto Composto Circulatório é proibido pela Anvisa
Anvisa recebeu denúncia do Conselho Regional de Farmácia – CRF do Rio Grande do Sul sobre a comercialização do produto Composto Circulatório (Ginko Biloba, Castanha da Índia, Hamamélis, Chá de Bugre, Tansagem, Alecrim do Campo e Malva) que não tem registro da Agência. A empresa que supostamente fabrica esse produto, J.A.S Campos – Ltda não possui CNPJ. A comercialização do produto é irregular. A Agência determina, portanto, a proibição da fabricação, distribuição, divulgação, comercialização e uso do produto bem como a apreensão das unidades do produto. Lote de azeite suspenso A Anvisa proibiu a distribuição e comercialização do lote 16D18…
Aprovado mais um novo medicamento para diabetes tipo 2
A Anvisa registrou mais um novo produto biológico para o tratamento de diabetes mellitus tipo 2. O registro do medicamento Xultophy, inédito no Brasil, foi aprovado pela Agência Sanitária e publicado no Diário Oficial da União (DOU) desta segunda-feira (3/4). O Xultophy, um composto formado entre a insulina degludeca + liraglutida, é indicado para o tratamento de adultos com diabetes mellitus tipo 2. O medicamento quando combinado com hipoglicemiantes orais auxilia no controle glicêmico do paciente. Como o Xultophy funciona O Xultophy atua em conjunto com outros hipoglicemiantes orais quando estes por si só ou combinados com um antagonista dos…
Suspensos nove lotes do medicamento Tevacarbo
A Agência Sanitária suspendeu a distribuição, comercialização e uso de nove lotes do produto Tevacarbo (carboplatina). A empresa Teva Farmacêutica Ltda, que fabricou tais lotes, encaminhou um pedido de recolhimento voluntário após constatar o uso de um fornecedor do princípio ativo carboplatina diferente do registrado na Anvisa. Os lotes do medicamento, indicado para o tratamento de estados avançados do carcinoma de ovário de origem epitelial e para o tratamento do carcinoma de pequenas células de pulmão, deverão ser recolhidos do mercado. Confira detalhes dos produtos suspensos e quais são os lotes em questão: Tevacarbo 10mg/ml, 15ml, lotes 15H28KC, 15H28KK e…
Proibida venda online de Cytotec
A divulgação e comercialização irregular do Cytotec (misoprostol), medicamento sem registro no Brasil, motivou a proibição da venda em um determinado website. A medida foi publicada no Diário Oficial da União (DOU), nesta terça-feira (21/3). Toda e qualquer venda de medicamentos à base da substância misoprostol é restrita a estabelecimentos hospitalares devidamente cadastrados e credenciados. Mas a marca comercial utilizada nesses ambientes, os serviços de saúde, é o Prostokos, medicamento registrado na Anvisa. A substância misoprostol faz parte da lista de substâncias sujeitas a controle especial, da Portaria 344/1998, norma atualizada regularmente pela Anvisa, sempre que uma droga nova surge ou que…
Empresa e produto sem autorização são proibidos
O produto Composto Sexual-25g-PER foi proibido pela Anvisa nesta sexta-feira (24/03). A empresa Sônia Maria Lopes Mendes não possui Autorização de Funcionamento da Agência e comercializava de maneira clandestina o produto não registrado. O produto clandestino era divulgado na internet. A Anvisa, assim, determina a proibição da fabricação, distribuição, divulgação, comercialização e uso do produto Composto Sexual-25g-PER pelo site da empresa ou por qualquer outro meio, em todo território nacional. Confira a resolução RE 780/17 publicada no Diário Oficial da União (DOU). Fonte: ANVISA
Produtos sem registro são interditados
A Anvisa proibiu a comercialização dos produtos Phospho (2-AEP) da empresa NewLife e Resveratrol + EA da empresa Life Plus World, ambos sem registros ou cadastros sanitários. As duas empresas não têm cadastro CNPJ ou Autorização de Funcionamento (AFE). Além disso, as propagandas encontradas nos sites eletrônicos atribuíam propriedades terapêuticas aos produtos, o que os caracteriza como passíveis de registro como medicamentos. As resoluções RE 779/17 e RE 781/17 determinam a proibição da fabricação, distribuição, divulgação, comercialização e uso de ambos os produtos em todo o território nacional. A Anvisa determinou, ainda, pela apreensão das unidades dos produtos no mercado brasileiro. Fonte: ANVISA
Publicidades irregulares são suspensas pela Anvisa
Após receber denúncias, a Anvisa encontrou e suspendeu propagandas irregulares da empresa registrada como Michel Gaspar da Silva ME, de nome fantasia OITI Indústria e Comércio de Produtos Naturais. E também da empresa Landelino Pereira – ME, de nome fantasia Chá & Cia. De acordo com as denúncias, as empresas veicularam, em diversas mídias, propagandas que atribuíam propriedades terapêuticas, de saúde e funcionais não permitidas pela Agência aos produtos produzidos por elas. Desta forma, foi determinada pelas resoluções RE 777/17 e RE 778/17 a suspensão de todas as publicidades e propagandas não autorizadas da empresa Michel Gaspar da Silva – ME e da empresa…
Produtos de empresa indiana tem a importação proíbida
A Anvisa determinou a proibição da importação de todos os medicamentos fabricados pela empresa Hospira Healthcare Índia Pv. Ltd. A empresa indiana teve o Certificado de Boas Práticas de Fabricação cancelado por descumprimento de práticas sanitárias motivando, assim, a medida de interesse sanitário. A empresa Hospira Healthcare Índia Pv. Ltd é suspeita de violação das Boas Práticas de Fabricação, além de diferentes não conformidades, tais como: -Realização de ensaios no Controle de Qualidade de matérias-primas e produto acabado em desacordo com o procedimento operacional padrão do método; -Manipulação de testes para atingir um resultado satisfatório; -Não investigação de desvios de…
Lote de Diazepam da Santisa Laboratório é suspenso
O lote 20101816 do medicamento Diazepam 10mg-2mL, solução injetável, foi suspenso pela Anvisa nesta quarta-feira (22/3). A empresa fabricante, Santisa Laboratório Farmacêutico S/A, enviou um comunicado de recolhimento voluntário após recebimento de laudo de análise insatisfatório no quesito rotulagem. A Agência determinou, assim, a suspensão da distribuição, comercialização e uso do medicamento Diazepam 10mg-2mL, solução injetável, lote 20101816. Determinou-se ainda que a empresa fabricante promova o recolhimento do estoque do mercado. Confira a resolução RE 758/17 publicada no Diário Oficial da União (DOU) nesta quarta-feira (22/3). Propaganda ilegal de medicamentos manipulados O material publicitário de medicamentos manipulados divulgados em um website da…
Medicamentos, propagandas e produtos suspensos
A Anvisa recebeu laudo de análise fiscal enviado pelo Laboratório Central do Estado do Paraná (LACEN-PR) com resultados insatisfatórios para o medicamento Rialcool (álcool etílico 70%) com 10 ml, da empresa Indústria Farmacêutica Rioquímica LTDA. Os resultados foram insatisfatórios nos ensaios de PH, aspecto e grau alcoólico, PH e grau alcoólico, aspecto e PH, e aspecto, PH e grau alcoólico. A Resolução-RE nº 534 determina a interdição, em todo o território nacional, dos lotes abaixo: Lotes Validade R1500364 30/01/2018 R1502881 30/06/2018 R1501352 31/03/2018 R1500984 28/02/2018 R1500078 30/01/2018 Paracetamol A Anvisa suspendeu também a distribuição, comercialização e uso do medicamento Dor-sanol…
Proibidos suplementos alimentares irregulares
O produto Intelimax IQ, 30 cápsulas de 500mg, da empresa Laboratório Gileadelab Ltda traz na lista de ingredientes o levedo de cerveja e no rótulo a informação de que se trata de Suplemento Vitamínico e Mineral, que não necessita de registro. No entanto, a presença do ingrediente levedo de cerveja coloca o produto na categoria de Novos Alimentos ou Novos Ingredientes que necessitam de uma avaliação antes da venda. Além da proibição da fabricação, distribuição e comercialização do produto, em todo território nacional, a Agência determina, pela Resolução RE nº 541, que a empresa recolha todo o estoque do produto disponível…
Anvisa publica nota sobre fosfoetanolamina como suplemento alimentar
A respeito das notícias veiculadas recentemente, pela imprensa e redes sociais, de que a fosfoetanolamina será comercializada como suplemento alimentar, a Anvisa esclarece que: Jamais foi protocolado, junto à Anvisa, qualquer pedido de registro da fosfoetanolamina, seja na forma de suplemento, seja na forma de medicamento. A fosfoetanolamina não é uma substância proibida, mas, para ser comercializada, de acordo com a legislação brasileira, e em conformidade com as regras praticadas em todos os países desenvolvidos do mundo, precisa estar registrada na Anvisa. Para que “suplementos” à base de fosfoetanolamina possam ser comercializados no Brasil, é necessário que esses produtos não…
Rastreabilidade: aberta Consulta Pública sobre o tema
A Anvisa abriu a Consulta Pública n° 311, de 15 de fevereiro de 2017, para contribuições da sociedade ao texto que servirá como base da proposta de revisão da RDC 54/2013, que normatiza a implantação do Sistema Nacional de Controle de Medicamentos. Na prática, isso significa a elaboração das diretrizes para a rastreabilidade de medicamentos na cadeia dos produtos farmacêuticos. Os interessados em contribuir têm, a partir de hoje, data em que a abertura da CP foi publicada no Diário Oficial da União, 30 dias para enviar seus comentários e sugestões. O diretor-presidente da Anvisa, Jarbas Barbosa, comemora a iniciativa:…
Boletim Anvisa
Anvisa mantém posição: medicamento genérico é seguro A Anvisa foi novamente citada pelo Programa Fantástico, da rede Globo, na edição deste domingo (05/02), em matéria intitulada “Anvisa questiona teste dos remédios genéricos, mas comete imprecisões”. A reportagem discute pontos da nota emitida pela Agência em razão de matéria anterior, onde o Fantástico levantou dúvidas sobre a qualidade dos medicamentos genéricos comercializados no Brasil. Ao programa e, principalmente, ao consumidor, a Anvisa mantém seu posicionamento: os medicamentos genéricos a que os brasileiros têm acesso são seguros e os testes realizados pelo laboratório Cedafar, da UFMG, são insuficientes para atestar se um…
Vigilância Sanitária atualiza taxas de fiscalização
Foi publicada na edição desta segunda-feira (30/01) do Diário Oficial da União a Portaria Interministerial Fazenda-Saúde 45/2017, que atualiza os valores da Taxa de Fiscalização de Vigilância Sanitária (TFVS). A portaria regulamenta o disposto na Lei 13.202, de 8 de dezembro de 2015, a qual autoriza o Poder Executivo a fazer atualização monetária dos valores de taxas federais, dentre elas a TFVS. A atualização dos valores da TFVS tem como base a data da instituição de cada fato gerador, por isso o índice é variável de acordo com cada hipótese de incidência do tributo. A atualização observa o limite de…
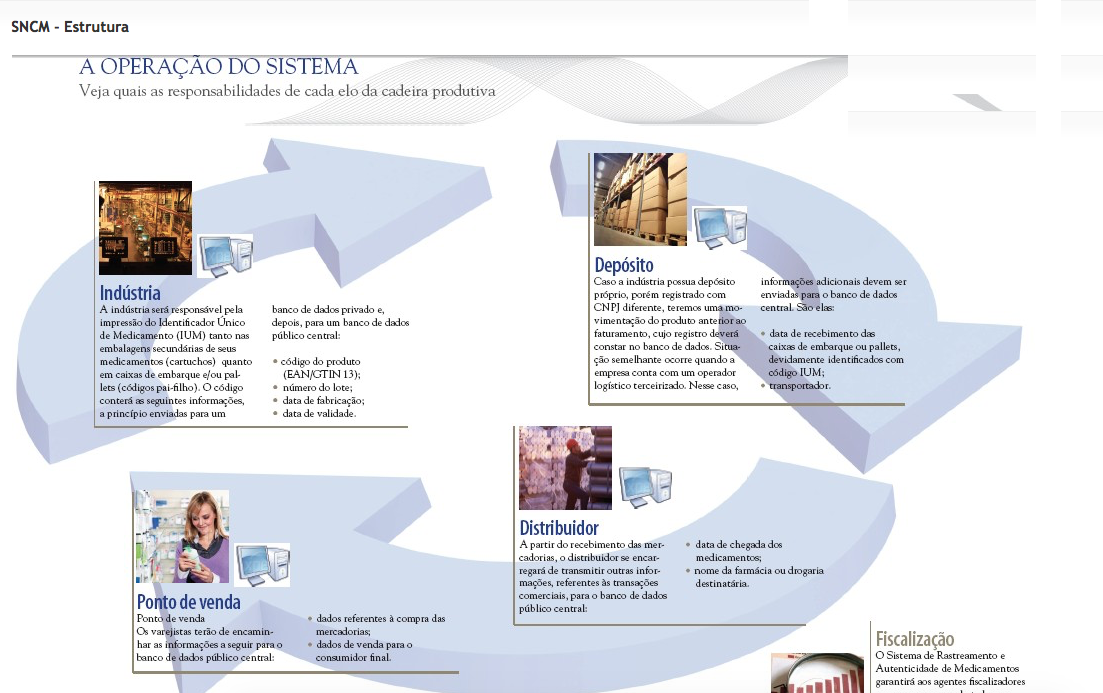
Anvisa cria GT sobre Sistema de Controle de Medicamento
A Anvisa vai instituir um Grupo de Trabalho (GT) para formular um Plano de Ação para o planejamento e execução de ações da Fase Experimental de implantação do Sistema Nacional de Controle de Medicamentos (SNCM). A Portaria foi aprovada na última Reunião da Diretoria Colegiada (DICOL), ocorrida nesta terça-feira (17/1) e será publicada no Boletim de Serviço (publicação interna), em breve. O SNCM é o sistema que irá monitorar todo medicamento produzido, dispensado e vendido no Brasil. A Lei 11.903 dispõe sobre o sistema e prevê o acompanhamento do medicamento em toda a cadeia produtiva, desde a fabricação até o…
Sabonete antisséptico Cinord é proibido
O sabonete antisséptico Cinord foi proibido pela Anvisa nesta segunda-feira (16/01). De acordo com autoridades sanitárias da Agência, o produto fabricado pela Cinord Sudeste Química Ltda era comercializado com uma formulação de um registro já vencido. Além disso, a formulação do sabonete possuía uma concentração de um conservante químico acima do permitido pela legislação sanitária. O produto portanto teve a fabricação, distribuição, comercialização e uso proibido. A Agência Sanitária declarou ainda o recolhimento de todo o estoque no mercado do cosmético em questão. A resolução RE 115/17 foi publicada no Diário Oficial da União (DOU). Fonte: ANVISA